
正大丰海首个自主研发1类创新药奥达替尼上市申请获CDE受理
发布时间:2026-02-06浏览次数:
正大丰海首个自主研发1类创新药奥达替尼上市申请获CDE受理
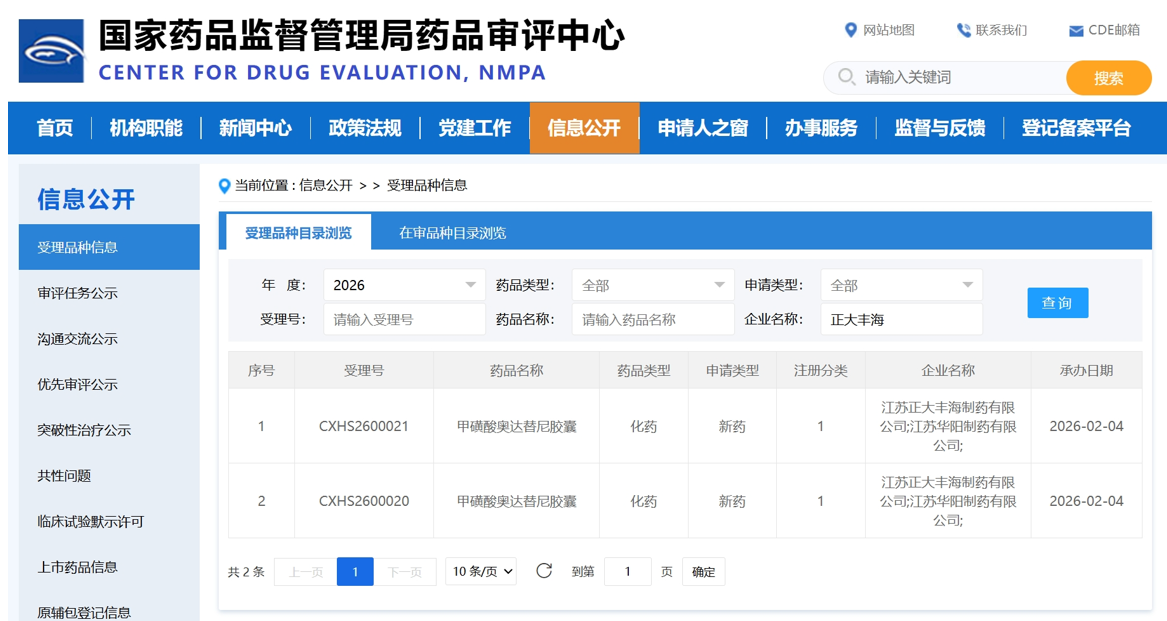
近日,江苏正大丰海制药有限公司自主研发的1类创新药——甲磺酸奥达替尼胶囊(Adonertinib,FHND9041)的新药上市申请,已正式获得国家药品监督管理局药品审评中心(CDE)受理。这是公司首个申报上市的1类新药,标志着正大丰海多年坚持自主创新的科研征程迎来里程碑式突破。
直面重大临床需求,推动更优治疗选择
肺癌是我国发病率与死亡率均居前列的恶性肿瘤。2022年数据显示,我国新发肺癌病例约106.06万例,占全部恶性肿瘤发病的22.0%,其中非小细胞肺癌(NSCLC)约占80%—85%。在亚洲人群中,EGFR突变较为常见,而外显子19缺失(19del)是其中的重要亚型之一,临床治疗仍存在持续优化与提升的空间。
奥达替尼属于第三代EGFR抑制剂,拟用于EGFR外显子19缺失(19del)的局部晚期或转移性非小细胞肺癌成人患者的一线治疗。该药物旨在为患者提供疗效更持久、安全性更友好的治疗新选择,有望进一步改善该类患者的生存预后与生活质量。
关键III期临床研究数据表现亮眼
本次上市申请获受理,主要基于FHND9041-III-01临床研究取得的积极结果。该研究是一项随机、阳性对照、开放的III期临床试验,旨在评估奥达替尼一线治疗EGFR突变相关局部晚期或转移性非小细胞肺癌的有效性与安全性。
研究结果显示,在EGFR 19del非小细胞肺癌患者中,主要终点经BICR评估的中位无进展生存期(mPFS)为26.05月,较对照组延长了9.52月,展现出明确的统计学意义与临床价值。与同类疗法公开数据相比,该结果亦显示出良好的竞争力。
在安全性方面,奥达替尼总体耐受性良好,大多数不良反应为1或2级;且无患者因为QT间期延长不良反应导致降低剂量、暂停本品治疗或永久停用本品,安全性特征较为清晰可控。
十年坚守,让创新成果稳步抵达患者
创新药研发,如同攀登未知险峰,既需系统布局、步步为营,也考验着企业在高投入、长周期与高风险中的持续定力。正大丰海始终坚持以创新为根本动力,持续加大研发投入、建强创新团队、夯实技术平台,沿着一条需要坚定信念的路径,一寸一寸扎实完成从0到1的突破,稳步推进从1到上市的进程。
此次奥达替尼新药上市申请获受理,不仅是公司从“仿创结合”迈向“创仿结合”的重要里程碑,更是正大丰海十年如一日深耕创新药的阶段性性答卷。这一进展的背后,正是企业在行业变局中始终保持的战略定力与穿越周期的内在韧性。
面向未来,公司将继续以患者需求为中心,稳步推进后续审评进程与产业化准备,以更高标准推进质量体系建设与合规管理,推动这把“十年磨就之剑”早日获批上市、惠及患者,为我国创新药高质量发展贡献更坚实的企业力量。





 苏公网安备 32098202000163号
苏公网安备 32098202000163号